以下文章來源于:藥智網(wǎng)
中國創(chuàng)新藥步入“商業(yè)化為王”的新階段����,創(chuàng)新藥故事的落腳點回歸到商業(yè)盈利能力上。隨著2023年Q1季報的陸續(xù)發(fā)布����,國內(nèi)創(chuàng)新藥賽道將迎來重要標(biāo)志的里程碑事件�����。一直霸占創(chuàng)新藥收入“一哥”位置的恒瑞�����,將迎來百濟(jì)神州的全線沖擊�����。2022年�����,預(yù)計百濟(jì)神州與恒瑞醫(yī)藥創(chuàng)新藥收入的差距將在20億元以內(nèi)���。若按照2023年Q1的增速核算,百濟(jì)神州有很大概率在2023年實現(xiàn)超越�。而創(chuàng)造增速爆量的核心引擎,正式具備“Best in class”潛力的BTK抑制劑澤布替尼�。而自從2012年百濟(jì)神州的BTK抑制劑的正式立項算起,已經(jīng)10年有余����。1993年,Bruton酪氨酸激酶(BTK)被發(fā)現(xiàn)����,作為B細(xì)胞受體信號通路中的關(guān)鍵激酶,具備治療血液瘤的巨大潛力�。2013年,全球第一款BTK抑制劑伊布替尼重磅來襲���,首次獲FDA批準(zhǔn)上市。它的出現(xiàn)為血液腫瘤帶來了革命性的進(jìn)展�����,使B細(xì)胞惡性腫瘤患者治療成功進(jìn)入無化療時代���。伊布替尼臨床的驗證也帶來了市場的認(rèn)可�����。上市第二年���,即突破10億美元�,晉升為新一代“重磅炸彈”�。2015年,艾伯維斥資210億美元重金收購Pharmacyclics�,獲得了伊布替尼在美國市場的商業(yè)化權(quán)利,創(chuàng)造了當(dāng)時投資并購的佳話�����。艾伯維的強(qiáng)勢入局����,攪動了BTK抑制劑的研發(fā)格局。阿斯利康���、吉利德�、小野制藥����、禮來紛紛加碼,國內(nèi)企業(yè)百濟(jì)神州�、諾誠健華發(fā)起沖鋒�。截止2023年����,全球共有6款BTK抑制劑獲批上市。分別為強(qiáng)生/艾伯維的伊布替尼���、阿斯利康的阿卡替尼����、百濟(jì)神州的澤布替尼�����、吉利德/小野制藥的tirabrutinib�、諾誠健華的奧布替尼、禮來的pirtobrutinib����。Pirtobrutinib在2023年獲得FDA加速批準(zhǔn)�����,是首個獲批上市的可逆非共價BTK抑制劑����,具有克服耐藥性的潛力�。6款BTK抑制劑中����,3款已在中國上市。分別是艾伯維和強(qiáng)生的伊布替尼�����、百濟(jì)神州的澤布替尼和諾誠健華的奧布替尼�����,均被納入醫(yī)保目錄����。在伊布替尼的強(qiáng)勢帶動下,全球BTK抑制劑市場在2022年已超過110億美元����。依靠著先發(fā)上市的優(yōu)勢,強(qiáng)生/艾伯維賺的盆滿缽滿����。阿卡替尼�、澤布替尼上市后也不甘示弱���,以每年翻一番的態(tài)勢“虎口奪食”����。
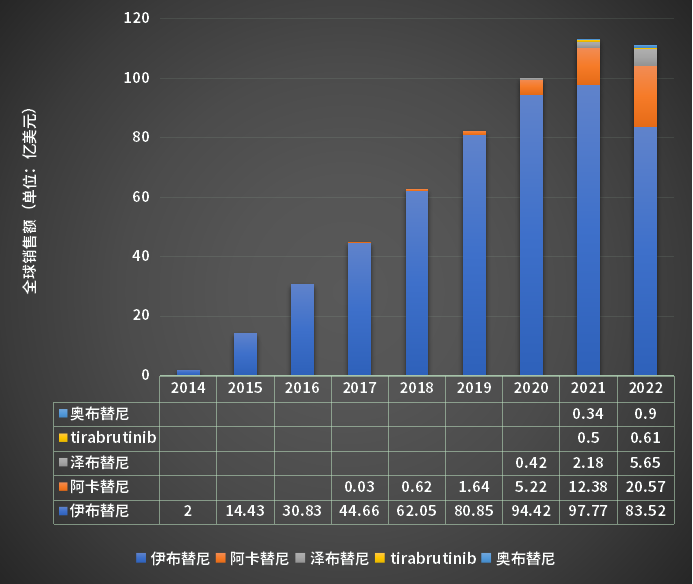
“打江山容易�����,守江山難”����,這句話形容伊布替尼特別貼切。2022年12月13日�,因為臨床獲益不佳,強(qiáng)生撤回了伊布替尼聯(lián)合苯達(dá)莫司汀與利妥昔單抗一線治療套細(xì)胞淋巴瘤(MCL)在歐洲的新適應(yīng)癥上市申請�;2023年4月6日,因為同樣的原因����,艾伯維和強(qiáng)生聯(lián)合宣布,計劃在美國自愿撤回伊布替尼的兩項適應(yīng)癥批準(zhǔn)�����。與強(qiáng)生/艾伯維擴(kuò)充江山不斷碰壁形成鮮明對比的是����,百濟(jì)神州的澤布替尼表現(xiàn)持續(xù)亮眼。在復(fù)發(fā)或難治性慢性淋巴細(xì)胞白血?����。–LL)或小淋巴細(xì)胞淋巴瘤(SLL)患者身上���,澤布替尼在關(guān)鍵療效指標(biāo)和安全性方面顯示出雙重優(yōu)效性�。這也是目前全球首個且唯一一款對比伊布替尼����,取得PFS與ORR雙重優(yōu)效性的BTK抑制劑。強(qiáng)生/艾伯維的退出���,百濟(jì)神州的進(jìn)擊���,讓澤布替尼開始逐步獨占細(xì)分適應(yīng)癥的市場,也帶來了澤布替尼的海外市場快速放量���。伊布替尼的“first in class”,一度貢獻(xiàn)了510億美元的銷售神話����,而澤布替尼展現(xiàn)出成為新一代BTK抑制劑藥王的潛力,又將分配多少杯羹�����?根據(jù)弗若斯特沙利文分析�����,全球BTK抑制劑的市場規(guī)模將以22.7%的年復(fù)合增長率達(dá)到200億美元�����。若樂觀估計���,澤布替尼按照過往2年的銷售增速����,則有望在2025年超越伊布替尼���,獲得至少一半以上的市場份額�。若平淡估計,澤布替尼在2025年占據(jù)全球10%的市場份額�,則銷售業(yè)績貢獻(xiàn)達(dá)到25億美元�����,折合人民幣170億元����,單品的銷售收入就有望問鼎“中國創(chuàng)新藥之王”。
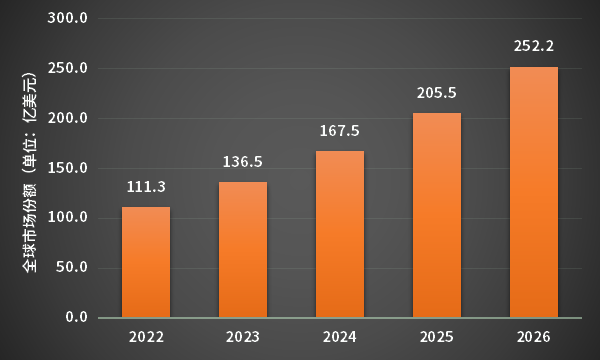
圖2 全球BTK抑制劑市場規(guī)模預(yù)測但是�����,藥王之路并不是那么好走的����,每一個藥王稱霸的路上,必然是“一將功成萬骨枯”�����。據(jù)藥智數(shù)據(jù)不完全統(tǒng)計���,全球已有近100家企業(yè)布局BTK抑制劑���,涉及140余個研發(fā)項目�,有38個項目已步入臨床階段�����。ACEA Biosciencesde的abivertinib已提交上市申請���,Principia Biopharma的rilzabrutinib���、默沙東的evobrutinib、賽諾菲的tolebrutinib����、羅氏的fenebrutinib以及諾華的remibrutinib五款藥物已進(jìn)入臨床三期階段,距離上市越來越近���。這些新上市的BTK抑制劑們����,也會對BTK的江山虎視眈眈���。
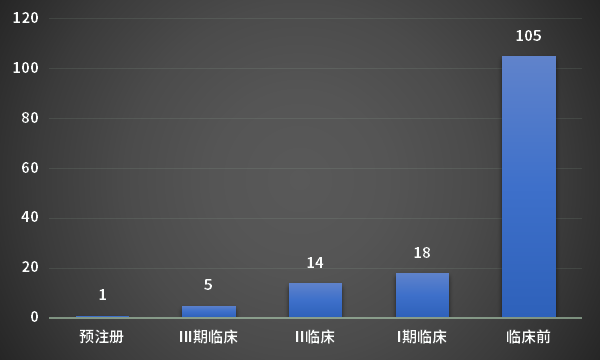
中國的創(chuàng)新藥已經(jīng)經(jīng)歷了國產(chǎn)新藥的元年�,license-out的元年。下一個元年將會是什么���?大概是“Best in class”的元年����。Best in class是一家創(chuàng)新藥藥企科技轉(zhuǎn)化能力的集中體現(xiàn)�����。而百濟(jì)神州���,則在澤布替尼中望見星辰大海的雛形。真正的星辰大海����,還需要實現(xiàn)“First in class”的突破以及“銷售藥王”的突破。創(chuàng)新藥的世界�,殘酷又美麗。作為一家企業(yè)����,盈利始終是核心特征。等到盈利到來的那一天�,百濟(jì)神州的星辰大海就觸手可及�。目前����,百濟(jì)神州有28款處于臨床研究階段的管線產(chǎn)品,超過50項臨床前研究項目�����,產(chǎn)品研發(fā)管線涵蓋了小分子藥����、單抗、雙抗����、ADC等多種類型。其中���,與合作伙伴共同開發(fā)的超過20款管線產(chǎn)品����,多款產(chǎn)品處在全球競爭格局第一梯隊的前列����。特別是在腫瘤領(lǐng)域�����,持續(xù)構(gòu)造“同類首創(chuàng)”���、“同類最優(yōu)”的競爭優(yōu)勢。預(yù)計在2023-2025年間�����,百濟(jì)神州在腫瘤領(lǐng)域?qū)崿F(xiàn)“收獲期”����。后續(xù)那些子彈會成為下一個澤布替尼���?我們拭目以待����。表1 百濟(jì)神州處于臨床研究階段的腫瘤藥物管線情況
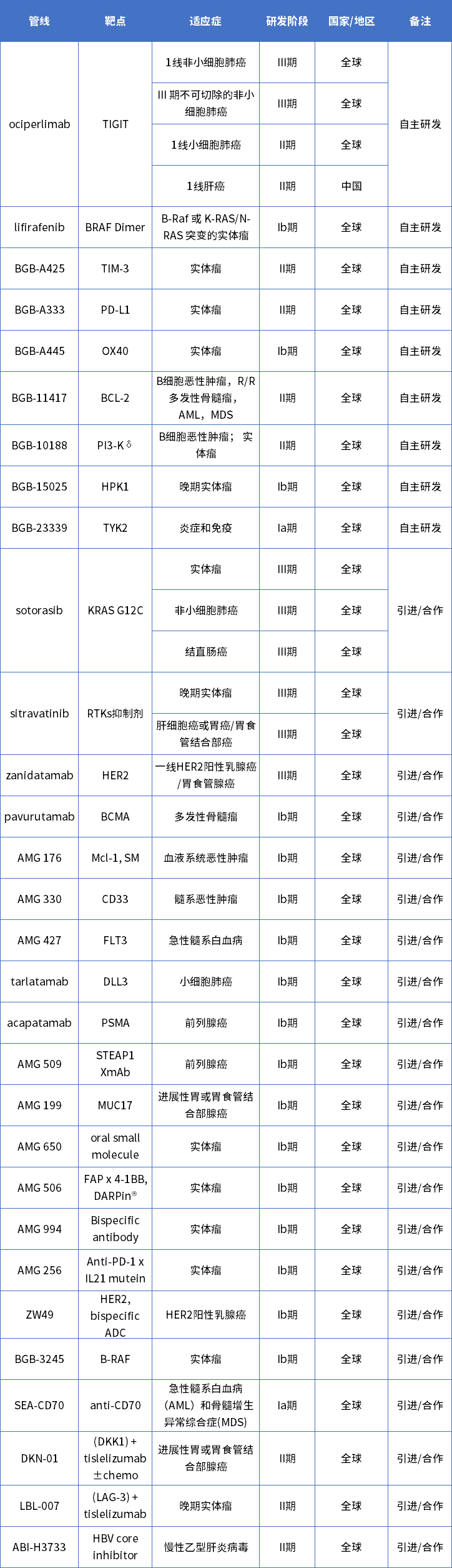
創(chuàng)新藥的成功屬于少數(shù)人�,每一個“藥王”的誕生,都要經(jīng)過臨床和市場的雙重驗證�。從引進(jìn)、合作開發(fā)���,到自主開發(fā)�����,再到技術(shù)�����、產(chǎn)品輸出�����,然后實現(xiàn)商業(yè)回報的豐收�,中國的創(chuàng)新藥企正在一步一腳印。百濟(jì)神州通過BTK抑制劑開始問鼎國內(nèi)創(chuàng)新藥一哥�,后續(xù)是否有可能在國內(nèi)第一梯隊沖擊全球big pharm?在這個始終是創(chuàng)新為王的時代����,讓我們共同期待。







